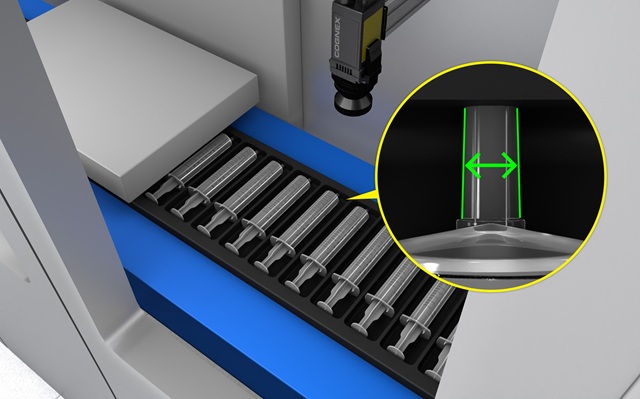
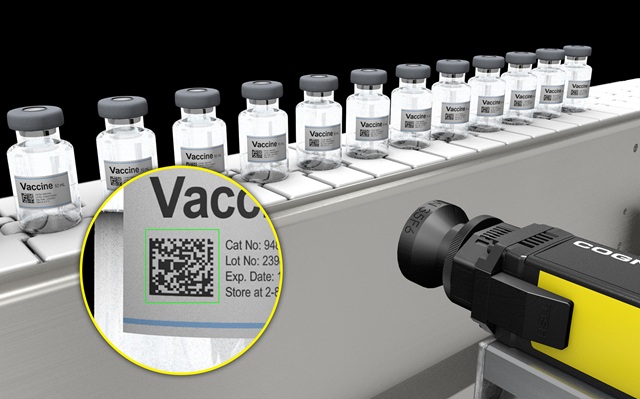
幸好,確保符合規範比普遍所瞭解的更簡單明瞭,支援所有合規要求,一般都提供最佳的驗證記錄保存程序。任何擁有符合 Part 11 規範的自動化品質管理系統 (QMS) 製造廠商,都將發現其可廣泛改善營運。所需要的只是稍加注意特定的機器視覺系統需求。
支援端對端 21 CFR Part 11 整備
In-Sight 8900 視覺系統具有諸如稽核記錄和單一登入 (SSO) 等進階功能,可協助製造商遵守 21 CFR Part 11。這些功能可確保安全、高效和可靠的電子記錄和簽名管理,同時提高整個營運的生產力和安全性。

稽核記錄
♦ 全面追蹤:自動記錄操作員操作的日期和時間戳。
♦ 高效的記錄檢索:輕鬆找到並存取記錄以供檢閱。
♦ 資料完整性:確保變更不會覆寫現有記錄,以防止資料遺失。

單一登入
♦ 透過 Microsoft Windows 進行集中管理:透過 Microsoft Windows 認證進行安全存取以簡化驗證,無需使用多個密碼。
♦ 訪問受控:僅限授權使用者訪問系統。
♦ 身份驗證:確認以電子方式簽署記錄的個人身份。
♦ 安全認證:使用強大的安全通訊協定保護系統,防止未經授權的訪問。
♦ 使用者專用設定:為單個使用者預設默認視圖,以提供更離散的控制
確保整個產品組合的法規遵循
Cognex 提供一系列符合 21 CFR Part 11 的視覺系統,讓您選擇最適合您的應用或環境的解決方案。
► In-Sight 2800
► In-Sight 3800
► In-Sight L38
► In-Sight 8900
參考資料
► 21 CFR Part 11和規基礎知識詳解